汇流新闻网记者陈钧凯/台北报导
用于骨折后固定的自费医材,艾斯博有限公司的“喜维克骨钉骨板系统”产品却爆出在尚未取得GMP认证前,擅自制造并供应7万多支钛合金骨钉骨板,食药署今(9)日公布流向,包括台大医院、北医、三总、成大医院等81家医疗院所,食药署也接获业者通报回收7万5299支骨钉、骨板,但数量却跟食药署掌握的对不上,将进一步厘清,不排除就回收不确实部分先行开罚。
艾斯博委托仕成精密科技股份有限公司在尚未取得GMP认证前,便擅自制造并供应7万多支钛合金骨钉骨板,消息曝光后,食药署9月10日即要求艾斯博启动产品回收。
食药署品质监督管理组副组长迟兰慧表示,今日已接获艾斯博公司缴交回收报告,共计回收7万5299支骨钉、骨板,并由高雄市卫生局协助清点,不过,食药署先前掌握仕成精密科技股份有限公司今年1月到7月制造量为7万4865支,数字明显兜不拢。
迟兰慧说,由于业者的同款产品同时委托2家业者生产,目前单就回收报告无法厘清产品哪些属于不合格者,须进一步厘清,若业者回收不确实可依法开罚20万到500万元罚锾;而违规制造部分则可开罚3万到200万元罚锾。
另一方面,食药署强调,已责成各地方卫生局至辖内医疗院所确认库存状况,问题产品于各医疗院所均已无库存。
迟兰慧指出,依现有掌握资料显示,今年1月至7月间使用“喜维克骨钉骨板系统”(卫部医器制字第004673号)许可证产品的医疗院所共有81家,食药署也已提醒医疗院所持续关注使用该许可证产品的病人,若有疑似不良反应发生,马上通报。
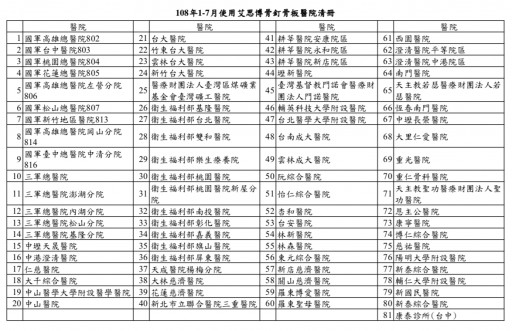
照片来源:食药署提供
【汇流笔阵】
CNEWS欢迎各界投书,来稿请寄至cnewscom2016@gmail.com,并请附上真实姓名、联络方式与职业身份简介。
CNEWS汇流新闻网:https://cnews.com.tw
【文章转载请注明出处】